化学疗法组合对癌细胞产生双重打击
如今,临床医生拥有200多种治疗多种癌症的药物,仅在2011年至2016年间就批准了68种药物。但是许多化学治疗剂提出了顽固的挑战:它们会导致严重的副作用,因为它们不仅杀死癌细胞,还会杀死健康的细胞。某些形式的癌症对药物产生抗药性;水溶性差的许多此类化学疗法显示出较低的生物利用度,导致药物向癌细胞的传递不足。
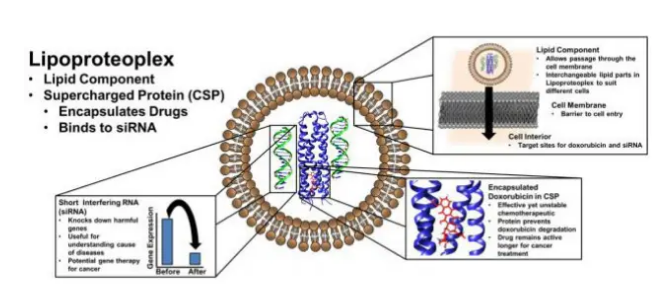
一种潜在的解决方案是化学治疗药物与遗传工程材料的协同组合,该遗传材料旨在中和赋予该药抗性的恶意基因,以及其他功能。
尽管有很多合成双基因和药物递送载体的例子,但纽约大学丹顿工程学院实验室开发的新型混合材料使用易于修饰的蛋白质来递送化学一两拳:它们结合了脂质“容器”用于转染—货物通过细胞膜的运输—以及易于结合的蛋白质胶囊,可以结合小的化学治疗分子和核酸。
由纽约大学丹顿化学与生物分子工程副教授Jin Kim Montclare领导的团队开发,他同时还是纽约大学文理学院的化学副教授以及纽约大学牙科学院生物材料的副教授。作为纽约州立大学下州分校的生物化学教授,这种混合的脂蛋白材料被称为脂蛋白复合物,既包括盘绕的带电荷的蛋白质大分子,也包括市售的转染剂Lipofectamine 2000。
因为研究人员设计了在表面带有大量正电荷和疏水性核心的蛋白质大分子,所以它很容易被带负电荷的短干扰RNA(siRNA)所修饰,siRNA是一种强大的工具,可以抑制引起耐药性并传播疾病状态的基因。也可作为疏水性化学治疗剂阿霉素的有效携带物,并减少毒性。
在《美国化学学会》杂志《生物大分子》中发表的研究中,研究小组详细介绍了暴露于MCF-7乳腺癌细胞系样品的脂蛋白复合物如何比单独的Lipofectamine 2000递送更多的阿霉素给靶细胞,从而大大降低了MCF-7细胞活力。他们还证明了杂交大分子在siRNA转染方面非常成功,使基因沉默了60%。
Montclare说,新的脂蛋白复合物的主要好处是易于修饰,这是研究人员研究其遗传调用行为随时间变化且随细胞系和患者而异的细胞的资产。脂质蛋白复合体就像混合和匹配成分的系统一样,使研究人员可以交换出一种超负荷的蛋白质或脂质成分以及任意数量的siRNA,以处理特定的细胞系和药物类型。
“与生产双重基因和药物递送系统的其他追求不同,这种方法不需要繁琐的化学合成程序;相反,我们可以生物合成增压蛋白质的任何变体。”她说。“这允许替换不同的siRNA分子和化学治疗药物以满足实验室的需求。”
在基于蛋白质的杂化材料的最新研究中,Montclare和她的合作者将工程化的增压蛋白质与转染试剂Fugene结合在一起。与单独的Fugene相比,该组合的DNA转染效率提高了八倍,而细胞毒性却可以忽略不计。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
预约试驾比亚迪元PLUS前,需注意以下几点:首先确认车型配置与预算是否匹配,了解车辆性能及续航信息。其次,...浏览全文>>
-
小鹏G7试驾前,新手需掌握以下步骤:1 预约试驾:通过官网或APP预约,选择合适时间和地点。2 准备证件:...浏览全文>>
-
预约别克GL8试驾,4S店提供专业且贴心的服务流程。首先,可通过电话或线上平台提前预约,选择合适的时间与车型...浏览全文>>
-
试驾奇瑞新能源QQ多米,新手可参考以下流程:1 预约试驾:通过官网或4S店预约,选择合适时间。2 到店接...浏览全文>>
-
试驾宝马X1,感受紧凑型SUV中的驾驶乐趣。轻踩油门,2 0T发动机迅速响应,动力输出平顺有力,提速迅猛。方向...浏览全文>>
-
福特烈马预约试驾,线上+线下操作指南:线上预约:访问福特官网或官方App,选择“试驾预约”,填写个人信息、...浏览全文>>
-
奥德赛试驾预约,简单几步,开启完美试驾之旅。只需三步,即可轻松完成预约:第一步,访问官网或拨打热线;第...浏览全文>>
-
想要快速锁定雷克萨斯ES的试驾名额,可采取以下方法:首先,访问雷克萨斯官网或使用官方APP,填写基本信息并提...浏览全文>>
-
想体验理想L8的智能与豪华?现在即可在线下预约试驾!作为一款中大型SUV,理想L8融合了家庭出行与科技感,搭载...浏览全文>>
-
试驾SRM鑫源摩托车时,需注意以下几点:首先,确认车辆状态,检查刹车、轮胎、灯光等是否正常。其次,选择安全...浏览全文>>
- 理想L8试驾线下预约
- 宝马X1预约试驾,4S店体验全攻略
- 华晨新日预约试驾,如何享受4S店的专业服务?
- 小鹏P7+试驾,开启完美驾驭之旅
- 元UP试驾预约,快速上手指南
- 金龙汽车预约试驾,新手试驾注意事项
- 蓝电试驾预约,如何快速预约并体验驾驶乐趣?
- 乐道L60试驾,如何在4S店快速预约?
- 小鹏MONA M03试驾,开启完美驾驭之旅
- 试驾别克昂科威,轻松几步,畅享豪华驾乘
- 云度新能源预约试驾有哪些途径
- 乐道L60试驾,如何在4S店快速预约?
- 哈弗大狗试驾,开启完美驾驭之旅
- 试驾深蓝汽车深蓝S05,线上+线下操作指南
- 日产奇骏试驾怎么预约
- 鸿蒙智行问界M9预约试驾,新手试驾注意事项
- 奇瑞艾瑞泽8预约试驾怎么预约
- 荣威预约试驾全攻略
- 坦克试驾,开启完美驾驭之旅
- 吉利银河预约试驾需要注意什么
