色素介导的翻译决定了神经细胞的命运
在胚胎和成人的大脑中,位于侧脑室周围脑室-室下区和海马齿状回亚颗粒区的生发壁上的特殊星形胶质细胞被认为是脑特异性神经干/祖细胞(Adams et al, 2004);Kriegstein & Alvarez-Buylla, 2009;Bayraktar等人,2014;Taverna等人,2014;邦德等人,2015)。这些具有星形胶质细胞谱系特征的神经上皮细胞衍生物,根据星形胶质标记物的apicobasal细胞结构和表达,分别被称为胚胎和成人大脑中的径向胶质细胞和B型细胞(Alvarez-Buylla et al, 2001;Merkle等人,2004年)。这些NSCs贯穿成人的一生,保留了产生大脑主要谱系的能力,包括神经元和神经胶质(Gage & Temple, 2013)。
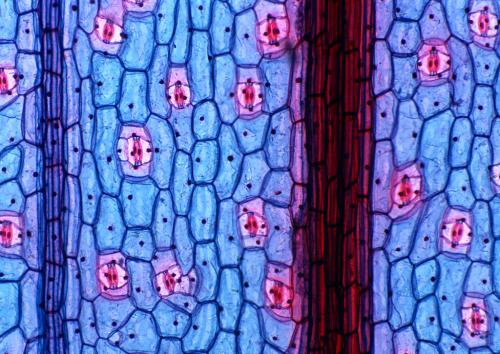
规范的NSC命运的问题从根本上是与细胞如何退出的未提交状态多功能干细胞,过渡到一个更直接的祖细胞的限制状态,并最终成为一个终末分化细胞与指定的命运,什么内在或外在分子机制造成这个过程?(Morrison et al, 1997;Edlund & Jessell, 1999)。神经祖细胞的固有异质性——这是发育和出生后老鼠大脑的一个特征——被认为是神经细胞和胶质细胞类型多样性的来源(Alvarez-Buylla et al, 2008;Rowitch & Kriegstein, 2010;Ihrie & Alvarez-Buylla, 2011年)。特别地,观察到不同类型的成人嗅球间神经元起源于不同的祖细胞群,说明了祖细胞异质性如何提供一种内在机制来驱动神经细胞的命运规范(Merkle et al ., 2007;Alvarez-Buylla等人,2008)。一群缓慢循环静止的NSCs(即,“静止的”NSCs, qNSCs)与有丝分裂活性的NSCs(即。在成年小鼠的心室-室下和亚颗粒区,“激活”NSCs, aNSCs)进一步强调了固有的转录水平的异质性,提供了一幅关于转录调控如何构成神经细胞命运规范的复杂图片(Codega et al ., 2014;Mich等人,2014;Llorens-Bobadilla等人,2015;Shin等人,2015)。尽管有证据支持干细胞命运和转录之间的相互联系,染色质重塑的直接或间接作用以及这些重塑对染色质动力学、转录级联和驱动细胞命运规范的下游事件的影响程度尚不清楚。
染色质重塑蛋白CHD5 (Li et al, 2014;Quan & Yusufzai, 2014)是一种编码于人1p36的抑癌基因(Bagchi et al ., 2007),该基因区域在包括神经母细胞瘤和胶质瘤在内的多种癌症中经常被删除(Bagchi & Mills, 2008)。Chd5强劲表现在终末分化postmitotic神经元(Vestin &钢铁厂,2013),也发现在海马祖细胞表达Sox3(伊根等,2013)——转录因子是神经祖细胞增殖和分化以及一些人口postmitotic神经元的前脑(王等人,2006)。Chd5也在胚胎日14.5 (E14.5)大鼠皮质分离的神经祖细胞中表达(Nitarska et al, 2016),表明它在神经发生的早期阶段起作用。有报道称,在晚期神经发生过程中Chd5的抑制阻碍了皮质迁移(Egan et al, 2013;Nitarska等人,2016)。然而,尚不清楚Chd5是否在早期作用,以限制NSC向有丝分裂活性状态的转变,如果是,这一瓶颈的扰动如何影响神经发生后期的细胞命运规范。使用从chd5缺陷新生儿大脑中分离出来的初级神经干细胞/祖细胞,我们发现在分化开始时过早激活NSC会改变细胞命运的决定,使星形胶质细胞比神经元谱系更受青睐。这些发现表明,在分化开始时的NSC激活过程对微调最终细胞命运至关重要,而染色质重塑因子Chd5在这一过程中起着关键作用。我们发现过早激活的chd5缺陷NSCs存在染色质扰动,并且超过一半的核糖体亚基蛋白编码基因显著上调,这表明chd5介导的染色质调控对于核糖体生物发生的转录调控至关重要。重要的是,在核糖体生物发生的不及时增强的驱动下,蛋白质合成的增加扰乱了关键的前膜转录因子Mash1在分化开始时的动态翻译调控异常表达,从而改变了神经元谱系的规范。这些观察揭示了决定细胞命运规范的多层次调控,并表明这些事件的时间协调在神经细胞命运的执行中起着中心作用。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
预约试驾比亚迪元PLUS前,需注意以下几点:首先确认车型配置与预算是否匹配,了解车辆性能及续航信息。其次,...浏览全文>>
-
小鹏G7试驾前,新手需掌握以下步骤:1 预约试驾:通过官网或APP预约,选择合适时间和地点。2 准备证件:...浏览全文>>
-
预约别克GL8试驾,4S店提供专业且贴心的服务流程。首先,可通过电话或线上平台提前预约,选择合适的时间与车型...浏览全文>>
-
试驾奇瑞新能源QQ多米,新手可参考以下流程:1 预约试驾:通过官网或4S店预约,选择合适时间。2 到店接...浏览全文>>
-
试驾宝马X1,感受紧凑型SUV中的驾驶乐趣。轻踩油门,2 0T发动机迅速响应,动力输出平顺有力,提速迅猛。方向...浏览全文>>
-
福特烈马预约试驾,线上+线下操作指南:线上预约:访问福特官网或官方App,选择“试驾预约”,填写个人信息、...浏览全文>>
-
奥德赛试驾预约,简单几步,开启完美试驾之旅。只需三步,即可轻松完成预约:第一步,访问官网或拨打热线;第...浏览全文>>
-
想要快速锁定雷克萨斯ES的试驾名额,可采取以下方法:首先,访问雷克萨斯官网或使用官方APP,填写基本信息并提...浏览全文>>
-
想体验理想L8的智能与豪华?现在即可在线下预约试驾!作为一款中大型SUV,理想L8融合了家庭出行与科技感,搭载...浏览全文>>
-
试驾SRM鑫源摩托车时,需注意以下几点:首先,确认车辆状态,检查刹车、轮胎、灯光等是否正常。其次,选择安全...浏览全文>>
- 理想L8试驾线下预约
- 宝马X1预约试驾,4S店体验全攻略
- 华晨新日预约试驾,如何享受4S店的专业服务?
- 小鹏P7+试驾,开启完美驾驭之旅
- 元UP试驾预约,快速上手指南
- 金龙汽车预约试驾,新手试驾注意事项
- 蓝电试驾预约,如何快速预约并体验驾驶乐趣?
- 乐道L60试驾,如何在4S店快速预约?
- 小鹏MONA M03试驾,开启完美驾驭之旅
- 试驾别克昂科威,轻松几步,畅享豪华驾乘
- 云度新能源预约试驾有哪些途径
- 乐道L60试驾,如何在4S店快速预约?
- 哈弗大狗试驾,开启完美驾驭之旅
- 试驾深蓝汽车深蓝S05,线上+线下操作指南
- 日产奇骏试驾怎么预约
- 鸿蒙智行问界M9预约试驾,新手试驾注意事项
- 奇瑞艾瑞泽8预约试驾怎么预约
- 荣威预约试驾全攻略
- 坦克试驾,开启完美驾驭之旅
- 吉利银河预约试驾需要注意什么
